Cerebraca® Wafer | 治療惡性腦瘤


Cerebraca® Wafer
小分子活性藥物EF-API-001與生物可分解高分子賦形劑結合製成 Cerebraca® Wafer,有助於強力毒殺腦癌細胞、活化免疫和降低化療藥物抗藥性。
- Cerebraca® Wafer是一種可用於高度惡性腦神經膠質瘤 (或稱惡性腦癌、惡性腦瘤) 的治療藥片,可直接植入腦部,通過局部高濃度、高滲透性、長時效緩慢釋放藥物持續達1個月,發揮多重靶向作用,有助於治療癌症,使癌細胞更容易被化療或免疫細胞殺死。
- 多形性神經膠母細胞瘤 (GBM) 是相當惡性的原發性腦瘤,一個月內最快可長大16倍,且手術切除腫瘤後的復發率高,目前仍無有效治療方式。
- Cerebraca® Wafer中的小分子活性藥物EF-API-001,它具有下列特性:
- 標靶Axl-1受體酪胺酸激酶:有效抑制腦瘤幹細胞生長和轉移。
- 抑制PD-L1免疫抑制檢查點:降低腫瘤微環境免疫抑制性,保持免疫細胞活性以毒殺腫瘤細胞。
- 降低MGMT修復DNA酶: 克服Temozolomide(化療藥物)抗藥性,使癌細胞能夠再次被化療藥物殺死。
- Cerebraca® Wafer及其內部成分小分子活性藥物、生物可分解高分子賦形劑均委託國際知名PIC/S GMP藥廠在台生產,以確保其高品質與可靠的無菌製程。
Cerebraca® Wafer針對復發高度惡性神經膠質瘤第I/IIa期臨床試驗
臨床試驗第I期
- 2020年8月完成台灣I期臨床試驗
- 整體試驗沒有發現與試驗藥物相關的不良反應
- 高劑量組別 (Cohort IV)
- 中位數整體存活期 (median OS) 累計已達26.2個月 (更新日期:2022/7),相較現有策略如格立得植入劑Gliadel® wafer (6.4個月)、帝盟多膠囊 (5.8個月)或癌思停注射液 (9.4個月)
- 6個月疾病無惡化存活率(PFS rate) 為100%
- Cancers 2022, 14(4), 1051; https://doi.org/10.3390/cancers14041051
- 臨床試驗第IIa期
- 2022年10月完成台灣IIa期臨床試驗收案
- 臨床研究報告 (Clinical Study Report) 預計於2024年3月底完成
Cerebraca® Wafer較能夠對抗復發型惡性腦膠質瘤中的癌幹細胞
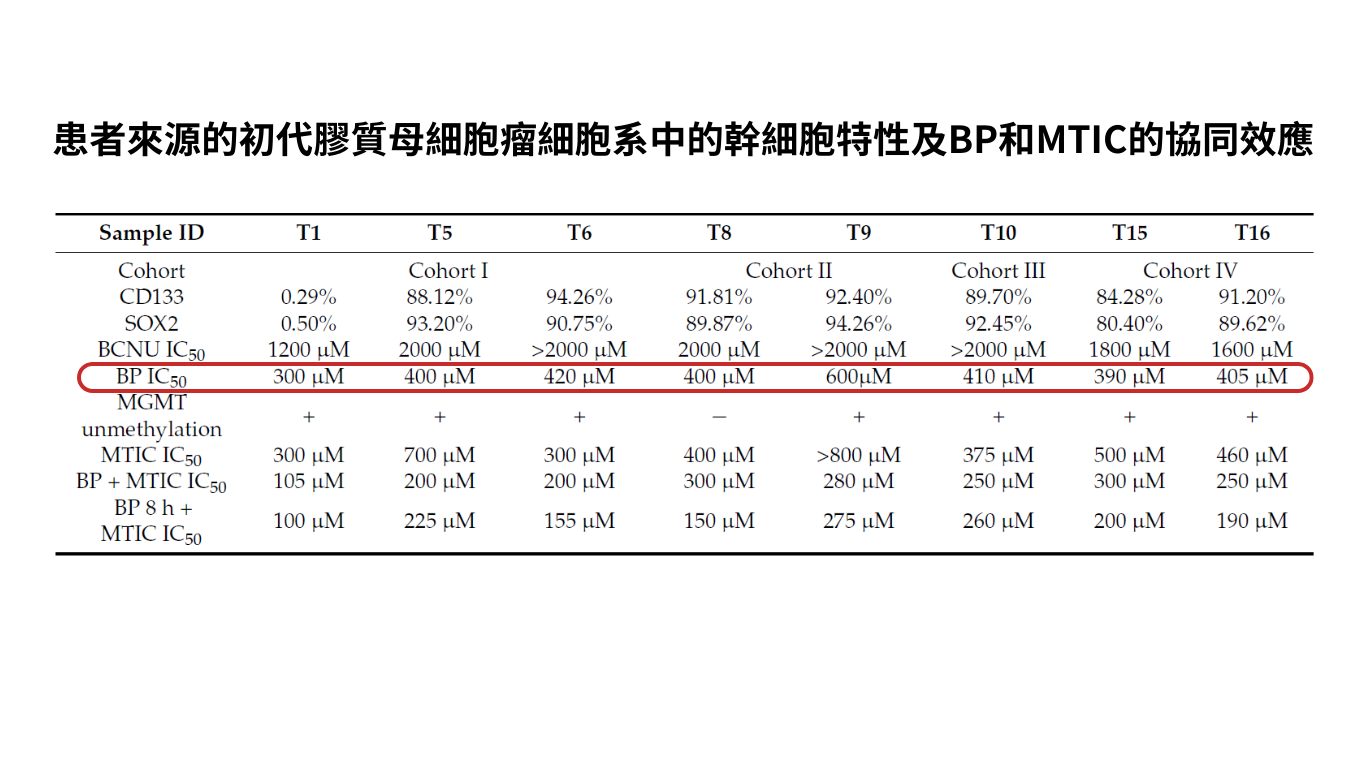
依據下表結果顯示,臨床試驗中獲得的八個初代惡性腦膠質瘤細胞株中,有七個細胞株呈現高表達癌幹細胞標誌物CD133和SOX2,這暗示著腫瘤復發時會有高比例的癌幹細胞產生。
BCNU (Gliadel wafer的有效成分) 抑制無腫瘤幹細胞株T1的IC50約為1200 uM。而有表達高癌幹細胞標誌物的GBM細胞在接受BCNU毒殺時需要有較高的IC50值 (≥1600 uM)。這結果可能與Gliadel wafer治療復發型惡性腦癌效果較差有限有關。
患者來源的初代膠質瘤細胞株使用BP來抑制時 (即EF-API-001) 的IC50比BCNU更低,顯示Cerebraca® wafer的活性成分BP比Gliadel wafer的活性成分BCNU更有抑制的效果。我們進一步證明BP的IC50約為BCNU的四倍低。
此外,Cerebraca® wafer較Gliadel wafer的給藥量幾乎達10倍之多 (每個wafer的藥物量分別為75和7.7 mg),這使得癌細胞有可能被BP所毒殺。
- 更多內容請見 Cancers 2022, 14(4), 1051; https://doi.org/10.3390/cancers14041051
我們致力於治療罕見癌症
罕見癌症是一種孤兒病,由於患者人數太少,如果缺乏公眾誘因和監管利益的話,治療孤兒病並不符合經濟效益。
- 我們的使命,是開發孤兒藥來治療罕見癌症。首先,由於缺乏有效的治療方法, 孤兒病的存活率偏低。 此外,同業推出次級貨品作競爭的風險亦較低。再者,開發孤兒藥可獲更多機會與全球製藥夥伴訂立許可協議,迅速獲得市場份額。
多型性神經膠母細胞瘤(GBM)
膠質母細胞瘤(GBM) 是最常見和致命的原發性腦瘤,該病對傳統放射治療和化療具有高度抗性,無法透過手術切除而有效地控制病情。由於GBM復發無法避免而且病情會急劇惡化,此病本質上被視為無法治愈。GBM的存活率很低,復發後平均預期壽命為半年。
在當前的GBM療法中,由於血腦屏障和血腦腫瘤屏障的阻礙,減弱了抗腫瘤藥物的效用,因此,如何將化療藥物有效地遞送至腫瘤位置是一項重大的挑戰。
為何鎖定多型性神經膠母細胞瘤(GBM)
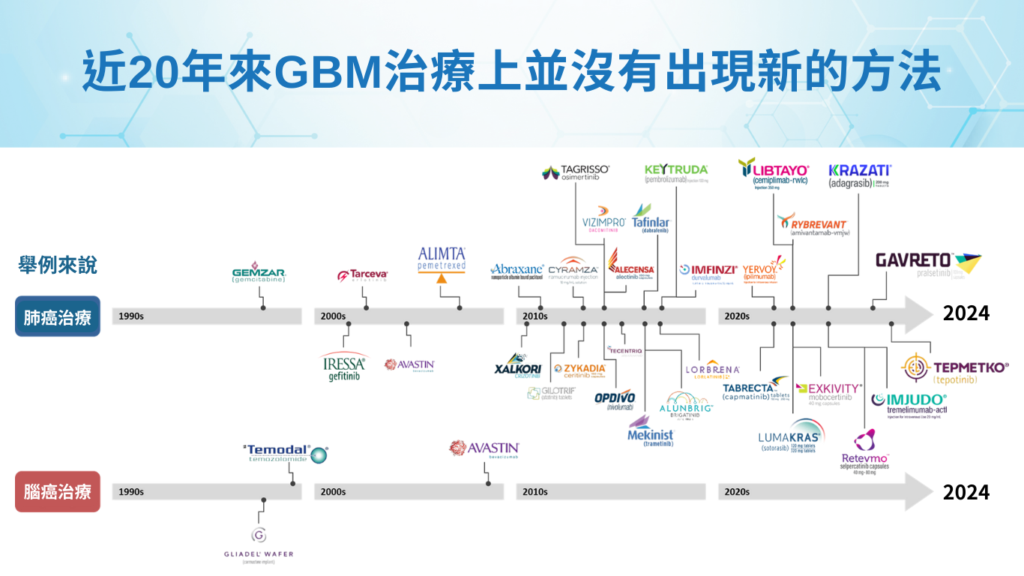
近20年來GBM治療上並沒有出現新的方法,相較於其他癌症治療,如肺癌,近20年來有超過30項藥物上市。
顯示全球在腦癌治療上面臨的困難與挑戰,這也是我們積極切入的主要原因。
我們的創新
利用人體免疫系統的力量
我們積極識別及開發能夠在多項指標上增強人體自然防禦能力的活性化合物,透過增強患者的免疫系統,削弱疾病,以增加疾病對藥物治療的脆弱性。
使用小分子藥物作為關鍵療法
由於小分子藥物的分子量相對較低,化學結構簡單,可預測其藥效和藥代動力,不但具備良好的安全概況,更可穿過細胞膜接觸細胞內靶點,並以多種形式配製。
以靶向藥物傳遞系統提高療效
我們使用靶向藥物傳遞平台來改善產品療效,例如局部緩慢釋放系統、全身給藥系統、滴丸製劑、皮膚外用製劑和注射用製劑等。
產品概況
產品名稱
Cerebraca® Wafer
治療病症
腦瘤(膠質瘤及腦膜瘤)
目標市場
北美洲、歐洲、亞洲、中國、日本及其他
市場規模
美國市場約值17.14億元美金*
市場競爭力
Gliadel® wafer和(Temozolomide,常見簡稱TMZ)的專利都已過期。
目標
成為手術聯合療法中的同類最佳藥物,佔據化療及免疫療法市場中15%的市場份額。
*2021年,全球腦腫瘤藥物市場約為23.1億美元,預計到2029年將增加到44.3億美元,在此期間的年複合增長率(CAGR)為9.0%。(來源:Fortune Business Insight (2021-2029))
Cerebraca® Wafer 如何治療腦癌?
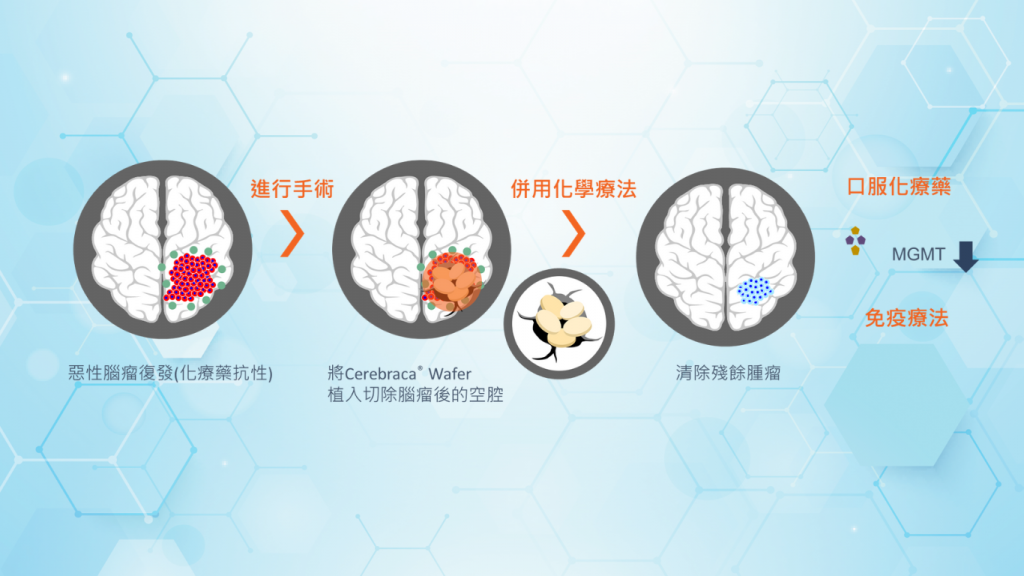
在手術中切除復發的腦瘤後,將Cerebraca® Wafer(植入藥片)植入空腔中。藥片會緩慢分解,並釋放小分子標靶藥物直接進入腫瘤,使病變局部能達到充分的藥物濃度,並在不損害其他組織的情況下,殺死在手術無法切除完全的癌細胞。
Cerebraca® Wafer 在治療腦癌上的優勢
■ 已取得US FDA 孤兒藥認證
可享有孤兒藥開發法案保障與優惠措施。
■ 延長預期壽命
臨床試驗第一階段期結果顯示,接受最高劑量的患者平均存活超過兩年,一名患者存活將近三年、目前正常生活中。
■ 低毒性
臨床試驗期間並無藥物相關不良反應—無腦腫、不引發癲癇、不影響傷口癒合。
■ 局部釋放藥物
植入後,錠片會緩慢分解,並釋放小分子標靶藥物直接進入腫瘤,使病變局部能達到充分的藥物濃度。
■ 多重靶向作用
小分子標靶藥物可在原位削弱癌症,使其高度脆弱、減低抗性,從而易於結合額外療法將其殺死。
■ 增強免疫力
抑制腫瘤細胞PD-L1,並激發免疫系統殺死腫瘤,從而逆轉傳統療法相關的免疫抑制性環境。
Cerebraca® Wafer 在治療復發GBM方面與傳統療法的比較

市場佔有率 (預估)

主要有效成份

活性藥理成分:EF-API-001
- 小分子
- 低毒性:Rat LD50 = 1,850 mg/kg
- PIC/S GMP認證藥品
EF-API-001是一種從天然產品研究中發現的小分子,可透過嚴格的GMP程序和控制中合成和製造。EF-API-001具有優良的安全性,能治療多種疾病,是一項令人興奮的發現。
EF-API-001的主要抗癌作用:抑制腫瘤生長、抑制幹性、抑制化療藥物抗性,以及刺激免疫反應。

賦形劑
- FDA 認證,可生物降解
- 具有良好生物相容性
- PIC/S GMP認證藥品
作用機制統整
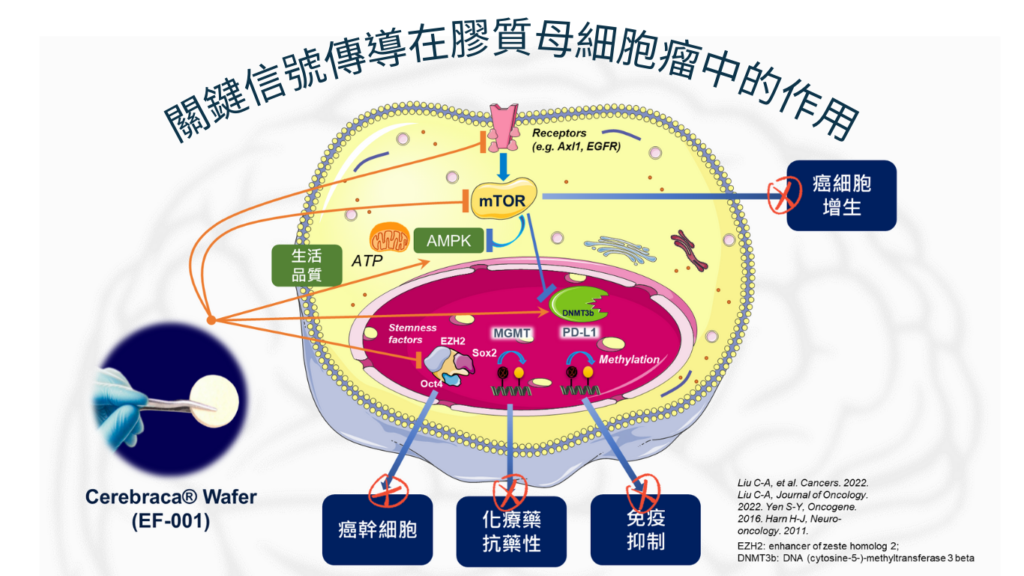
Cerebraca® Wafer是如何來抑制腦腫瘤復發與腦腫瘤惡化?
手術切除腦瘤後,直接將 Cerebraca® Wafer 植入摘除的GBM邊緣。其特點是可持續 30 天釋放藥物和達5公分的滲透深度,可以為癌症治療創造了高藥物濃度的環境。
Cerebraca® Wafer 是一種多功能藥物:
- 具有抑制受體酪氨酸激酶(Axl-1 和 EGFR)的潛力,從而阻止癌細胞與癌幹細胞的增殖。
- 抑制 Axl-mTOR 路徑和激活 AMPK 提高 ATP 水平,從而改善患者的生活質量。
- 它還能促進 MGMT 和 PD-L1 啟動子的甲基化,克服化療抗藥性,並將腫瘤微環境由冷並灶轉化為熱並灶而增強免疫活性。
臨床試驗現況
Cerebraca® Wafer治療惡性腦瘤臨床試驗一期試驗大有斬獲,受邀於ACNS演講,主講人:林欣榮 院長
Summary
- 長弘生技所開發的新藥Cerebraca® Wafer,在治療復發性惡性腦瘤的第一期臨床試驗中顯示出卓越的安全性和療效。
- 試驗涉及12名患者,接受最高劑量的患者平均存活時間超過19個月。
- Cerebraca® Wafer的設計是在手術後清除殘留的惡性腦瘤細胞,並在(Temozolomide,常見簡稱TMZ)的幫助下減少化療抗性。
- 目前復發性惡性腦瘤的標準治療效果有限,迫切需要新的治療方法。
成果 與 獲獎
2014 國家新創獎*
2015 美國FDA孤兒藥認證
2016 通過台灣生技新藥產業發展條例的資格
2016 美國FDA、台灣衛福部核准臨床試驗
2019 台北生技獎*
2019 神經外科醫師大會 – 被選為最高分新報告
2019 國家新創獎–新創精進獎*
2021 國家新創獎–新創精進獎*
2022 國家新創獎–臨床新創獎*
2023 NBRP DEMODAY – 投資人青睞獎
*台灣政府頒發獎項
專利佈局
學術期刊
- 2022 | Interstitial Control-Released Polymer Carrying a Targeting Small-Molecule Drug Reduces PD-L1 and MGMT Expression in Recurrent High-Grade Gliomas with TMZ Resistance
- 2022 | Biodegradable Controlled-release Polymer Containing Butylidenephthalide to Treat a Recurrent Cervical Spine Glioblastoma with Promising Result: a Compassionate Trial Report
- 2022 | Targeting the Axl and mTOR Pathway Synergizes Immunotherapy and Chemotherapy to Butylidenephthalide in a Recurrent GBM
- 2018 | Migration/Invasion of Malignant Gliomas and Implications for Therapeutic Treatment
- 2017 | n-Butylidenephthalide Regulated Tumor Stem Cell Genes EZH2/AXL and Reduced Its Migration and Invasion in Glioblastoma
- 2015 | Biodegradable Interstitial Release Polymer Loading a Novel Small Molecule Targeting Axl Receptor Tyrosine Kinase and Reducing Brain Tumour Migration and Invasion
- 2014 | Brain tumor senescence might be mediated by downregulation of S-phase kinase-associated protein 2 via butylidenephthalide leading to decreased cell viability
- 2013 | The Methanol Extract of Angelica sinensis Induces Cell Apoptosis and Suppresses Tumor Growth in Human Malignant Brain Tumors
- 2013 | (Z)-Butylidenephthalide restores Temozolomide sensitivity to Temozolomide-resistant malignant glioma cells by downregulating expression of the DNA repair enzyme MGMT.
- 2011 | Overexpression of the Orphan Receptor Nur77 and Its Translocation Induced by PCH4 May Inhibit Malignant Glioma Cell Growth and Induce Cell Apoptosis
- 2011 | Local Interstitial Delivery of z-Butylidenephthalide by Polymer Wafers against Malignant Human Gliomas
- 2011 | Butylidenephthalide suppresses human telomerase reverse transcriptase (TERT) in human glioblastomas
- 2010 | Extended O6-methylguanine methyltransferase promoter hypermethylation following n-butylidenephthalide combined with 1,3-bis(2-chloroethyl)-1-nitrosourea (BCNU) on inhibition of human hepatocellular carcinoma cell growth
- 2008 | Orphan Nuclear Receptor, Nurr-77 was a Possible Target Gene of Butylidenephthalide Chemotherapy on Glioblastoma Multiform Brain Tumor
- 2006 | The natural compound n-butylidenephthalide derived from Angelica sinensis inhibits malignant brain tumor growth in vitro and in vivo
- 2005 | Acetone extract of Angelica sinensis inhibits proliferation of human cancer cells via inducing cell cycle arrest and apoptosis
- 2005 | The antitumor effects of Angelica sinensis on malignant brain tumors in vitro and in vivo
合作與授權
長弘生物科技秉持開放的心態,持續尋找與國際藥廠或創投合作的機會。
請與我們聯繫 efbiotech@efbiotech.com