HK-001 | 治療漸凍症


HK-001 Soft Capsules
治療漸凍症
我們致力於治療罕見疾病
罕見癌症是一種孤兒病,由於患者人數太少,如果缺乏公眾誘因和監管利益的話,治療孤兒病並不符合經濟效益。
- 我們的使命,是開發孤兒藥來治療罕見疾病。首先,由於缺乏有效的治療方法, 孤兒病的存活率偏低。 此外,同業推出次級貨品作競爭的風險亦較低。再者,開發孤兒藥可獲更多機會與全球製藥夥伴訂立許可協議,迅速獲得市場份額。
漸凍症 (肌萎縮側索硬化症,Amyotrophic lateral sclerosis (ALS))
-
漸凍症的發病年齡為 40~70 歲,平均年齡為55歲。在美國每年新診斷人數約5000-6000名,在台灣每年新增300-500名。
-
約90%的漸凍症案例沒有明確的家族史或基因變異原因。剩餘的5-10%漸凍症案例稱為家族性漸凍症(Familial ALS,FALS),這些案例是由已知與漸凍症有關的突變基因遺傳而來。
-
無有效治療方式:目前漸凍症治療無有效的方式,僅能延緩病程、改善生活品質的方式。
-
致死率高:根據美國國家漸凍症協會的統計,患者通常在發病後平均存活約2至5年,但這可能因個體而異,僅有10%的患者能夠存活超過10年。
我們的創新
使用小分子藥物作為關鍵療法
由於小分子藥物的分子量相對較低,化學結構簡單,可預測其藥效和藥代動力,不但具備良好的安全概況,更可穿過細胞膜接觸細胞內靶點,並以多種形式配製。
利用人體免疫系統的力量
我們積極識別及開發能夠在多項指標上增強人體自然防禦能力的活性化合物,透過抑制 mTor標靶為抑制過強的自體吞噬作用等功效達到治療的目標。
以靶向藥物傳遞系統提高療效
我們使用靶向藥物傳遞平台來改善產品療效,例如局部緩慢釋放系統、全身給藥系統、滴丸製劑、皮膚外用製劑和注射用製劑等。
產品概況
Product Name
HK-001軟膠囊
Disease
漸凍症 (Amyotrophic lateral sclerosis,ALS)
Target Market
美國、法國、德國、義大利、西班牙、英國、日本等7個主要的國家,預估到2023年增加到3.7萬病患。
Market Size
預估2027年全球7個主要國家市場年約 USD 12億元
Competition Size
目前市場無真正能治癒ALS藥物
Objective Size
成為最佳ALS新藥,佔據市場中15%的市場份額。
HK-001軟膠囊
HK-001軟膠囊含有PIC/S GMP生產小分子活性藥物EF-API-001,透過標靶經由抑制 mTor與抑制過強的自體吞噬作用,達到延緩 ALS患者之發病進程。
- HK-001軟膠囊 為口服劑型,在動物試驗 (ALS小鼠,SOD1G93A小鼠) 的結果中可以看到下列2個改善的現象:
延緩漸凍症的發病進程:以 BBB scale (Basso, Beattie and Bresnahan scale) 運動量表小於15分作為發病的分界點,可看到口服 HK-001的漸凍症小鼠,發病的時間皆有所延後,優於對比藥物銳力得 (Riluzole)。
延長漸凍症的存活:口服 HK-001的漸凍症小鼠存活優於未治療組,亦優於對比藥物銳力得。
HK-001在治療ALS上的優勢
延緩發病進程
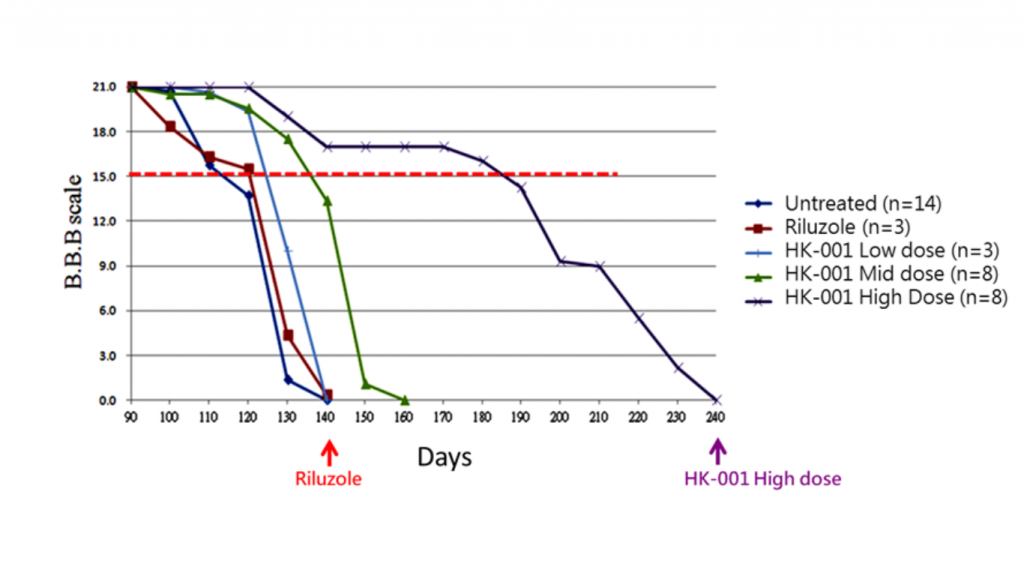
BBB scale < 15 時程
以 BBB scale小於15分作為發病的分界點,可看到口服 HK-001的漸凍症小鼠,發病的時間皆有所延後,優於對比藥物銳力得。
延長存活期
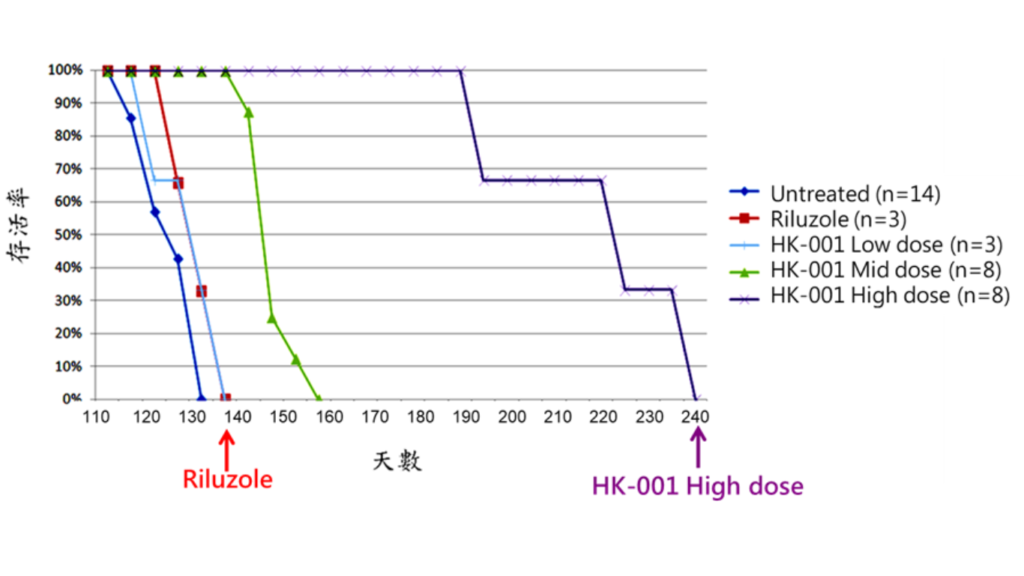
存活期
口服 HK-001的漸凍症小鼠存活優於未治療組,亦優於對比藥物銳力得。
HK-001作用機制 - 可抑制自噬 (Autophagy) 之過量表現
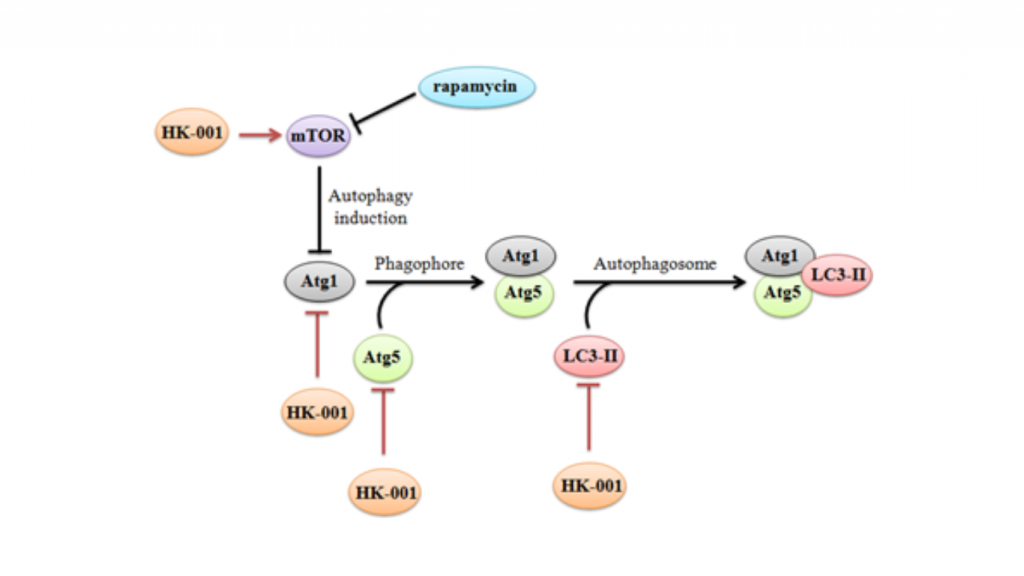
LC3-II之累積量與 autophagy之作用息息相關,且LC3-II蛋白之異常堆積也被認為是ALS病情惡化的主因之一。
利用 NSC-34-SOD1G93A細胞株進行實驗,可以發現HK-001能夠刺激SOD1G93A突變細胞株內之mTOR訊息傳遞活化,進而降低了LC3II之堆積。
由動物實驗的結果中也能發現 SOD1G93A小鼠之脊椎神經內LC3-II累積量較正常組要來的高,而經過HK-001治療後之小鼠能夠有較為治療組為高的 mTOR活性,且 LC3-II的累積量也降至接近 wild type組。
利用專一性抗體針對運動神經元染色,也觀察到HK-001治療組之運動神經元數目遠高於未治療組,且運動神經元數目與 BBB scale結果具有相關性。利用LC3-II-GFP基因轉殖鼠進行確認,也能夠發現給予HK-001藥物治療的小鼠體內之螢光強度下降。
證實了 HK-001延長 SOD1G93A小鼠之壽命主要是透過了磷酸化/活化 mTOR來調控 LC3-II堆積量以及其下游 autophagy之作用來達成延長 SOD1G93A小鼠壽命的功效。
關於銳力得(Riluzole)
是一種苯并噻唑類的口服藥物,為阻斷麩氨酸拮抗的神經傳導作用有關的藥物,麩氨酸本身是一種興奮性胺基酸,被認為與造成神經退化的興奮性毒性有關,但ALS的真正疾病致因並未獲得了解,此為可能的假設之一。
延長存活時間或延後使用機械呼吸器時間,仿單上說明對於末期ALS病患無療效。
臨床試驗結果顯示試驗組的存活期中位數17.7個月較安慰劑組的14.9個月來的高。
可能會出現一些副作用,例如衰弱無力、噁心、肝功能指數異常。約有14%的受試者在此藥物的臨床試驗期間因為這些副作用而放棄測試。
成果 與 獲獎
2014 獲得經濟部A+企業創新研發淬鍊計畫經費補助
2017 第十四屆國家新創獎 – 學研新創獎*
2018 臨床試驗IND申請獲得美國 FDA核准執行
2019 臨床試驗IND申請獲得台灣衛生福利部 (TFDA)核准執行
2020 獲得第十六屆國家新創獎 – 新創精進獎*
2021 獲得第十八屆國家新創獎 – 新創精進獎*
*台灣政府頒發獎項
專利佈局
學術期刊
- 2021 | n-Butylidenephthalide Modulates Autophagy to Ameliorate Neuropathological Progress of Spinocerebellar Ataxia Type 3 through mTOR Pathway
- 2018 | Advances in Patient-Specific Induced Pluripotent Stem Cells Shed Light on Drug Discovery for Amyotrophic Lateral Sclerosis
- 2016 | Autophagic down-regulation in motor neurons remarkably prolongs the survival of ALS mice
合作與授權
長弘生物科技秉持開放的心態,持續尋找與國際藥廠或創投合作的機會。
請與我們聯繫 efbiotech@efbiotech.com